Mes: marzo 2014
Número PI
El número pi, representado por la letra griega π, equivale a laconstante que relaciona el perímetro o longitud de unacircunferencia con su diámetro. Se trata de un valor con un infinito número de decimales, cuya secuencia comienza de la siguiente manera:
3,1415926535897932384626433832795028841…

Redondeado en 3,1416, pi es un número irracional -no puede representarse de forma fraccional-, frecuentemente utilizado en lasmatemáticas y en la física, además de en otras disciplinas como lageometría y la trigonometría.
Al cálculo de pi se han dedicado millones de horas desde que losantiguos egipcios, allá por el año 1600 a.C, ya concluyeran que existía relación entre la longitud y el diámetro de una circunferencia.
Griegos tan insignes como Arquímedes o Ptolomeoexperimentaron con polígonos de cientos de lados y circunferencias de decenas de unidades de radio para aproximarse al número pi con la mayor precisión posible. También lo hicieron en China e India, y más tarde enEuropa, continente en el que el francés Fabrice Bellard, a principios de 2010, consiguió establecer el record de decimales conocidos de pi en 2,7 billones.
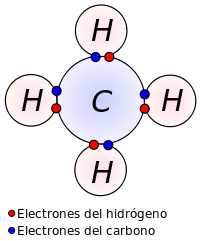
Un enlace covalente entre dos átomos o grupos de átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, comparten electrones del último nivel.1 La diferencia de electronegatividades entre los átomos no es suficiente.
De esta forma, los dos átomos comparten uno o más pares electrónicos en un nuevo tipo de orbital, denominado orbital molecular. Los enlaces covalentes se suelen producir entre elementos gaseosos o no metales.
El enlace covalente se presenta cuando dos átomos comparten electrones para estabilizar la unión.
A diferencia de lo que pasa en un enlace iónico, en donde se produce la transferencia de electrones de un átomo a otro; en el enlace covalente, los electrones de enlace son compartidos por ambos átomos. En el enlace covalente, los dos átomos no metálicos comparten uno o más electrones, es decir se unen a través de sus electrones en el último orbital, el cual depende del número atómico en cuestión. Entre los dos átomos pueden compartirse uno, dos o tres pares de electrones, lo cual dará lugar a la formación de un enlace simple, doble o triple respectivamente. En la representación de Lewis, estos enlaces pueden representarse por una pequeña línea entre los átomos.
Considérense átomos de hidrógeno, a medida que se aproximan entre sí, se van haciendo notar las fuerzas que atraen a cada electrón al núcleo del otro átomo, hasta que dichas fuerzas de atracción se llegan a compensar con la repulsión que los electrones sienten entre sí. En ese punto, la molécula presenta la configuración más estable.
Lo que ha sucedido es que los orbitales de ambos electrones se han translapado, de modo que ahora es imposible distinguir a qué átomo pertenece cada uno de los electrones.
Sin embargo, cuando los átomos son distintos, los electrones compartidos no serán atraídos por igual, de modo que estos tenderán a aproximarse hacia el átomo más electronegativo, es decir, aquel que tenga una mayor apetencia de electrones. Este fenómeno se denomina polaridad (los átomos con mayor electronegatividad obtienen una polaridad más negativa, atrayendo los electrones compartidos hacia su núcleo), y resulta en un desplazamiento de las cargas dentro de la molécula.
Se podría decir que al átomo más electronegativo no le gusta mucho compartir sus electrones con los demás átomos, y en el caso más extremo, deseará que el electrón le sea cedido sin condiciones formándose entonces un enlace iónico, de ahí que se diga que los enlaces covalentes polares tienen, en alguna medida, carácter iónico.
Cuando la diferencia de electronegatividades es nula (dos átomos iguales), el enlace formado será covalente puro; para una diferencia de electronegatividades de 1,9 el carácter iónico alcanza ya el 35%, y para una diferencia de 3, será del 49.5%.
Así pues, para diferencias de electronegatividades mayores de 3 el enlace será predominantemente de carácter iónico, como sucede entre el oxígeno o flúor con los elementos de los grupos 1 y 2; sin embargo, cuando está entre 0 y 1,9 será el carácter covalente el que predomine, como es el caso del enlace C-H. No obstante, según el químico Raymond Chang, esta diferencia de electronegatividad entre los átomos debe ser 2,0 o mayor para que el enlace sea considerado iónico.
Dependiendo de la diferencia de electronegatividad, el enlace covalente puede ser clasificado en covalente polar y covalente puro o apolar. Si la diferencia de electronegatividad está entre 0,4 y 1,7 es un enlace covalente polar, y si es inferior a 0,4 es covalente apolar.